|
ETUDE DU BMV PAR DIFFUSION DES RAYONS X AUX PETITS ANGLES
|
La Diffusion des Rayons X aux Petits Angles donne deux
types
|
I - Interactions entre particules virales en solution Spherical plant viruses: interactions in solution, phase diagrams and crystallization of Brome Mosaic Virus M. Casselyn, J. Perez, A. Tardieu, P. Vachette, J. Witz, H. Delacroix Acta Crystallographica Section D, 2001, Volume D57, pages 1799-1812 |
|
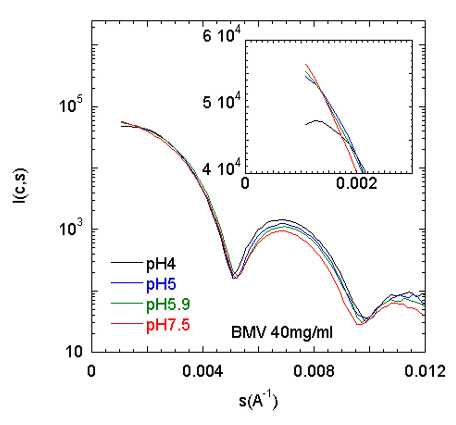
Effet du pH
|

|
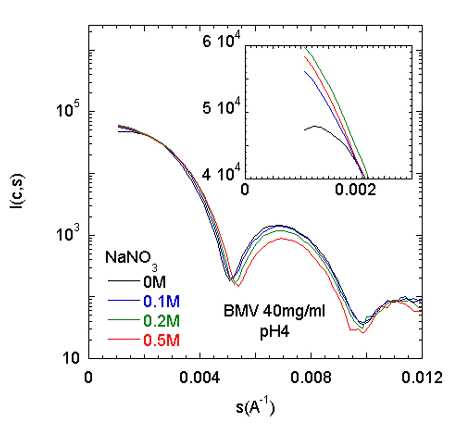
Effet des sels
Les
interactions peuvent également être modifiées
en écrantant les charges avec des sels. Nous avons utilisé
deux sels, l ’acétate de sodium et le nitrate de sodium
à différentes concentrations.
|
|
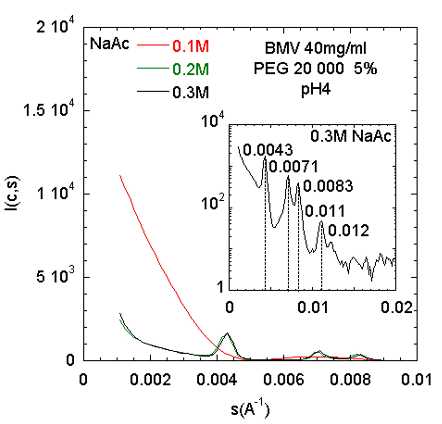
Effet du PEG
Le PolyEthyleneGlycol (PEG) est couramment utilisé dans la cristallisation des protéines. Nous avons utilisé deux tailles de PEG: 8000 et 20 000, à des concentrations allant de 3 à 10%, en présence ou en absence de PEG.
|